Hoy nos toca aprender sobre el elemento número 89: El actinio. Es el primero del grupo de los actínidos, esos 15 elementos que normalmente (Al menos desde mediados del siglo pasado, cuando Glenn Seaborg (Me voy a cansar de nombrarlo en los próximos elementos) y sus colegas de California remataron la Tabla Periódica, inventaron el concepto de actínido y dispusieron a éstos curiosos elementos en unas filas aparte) se colocan en una línea aparte en la Tabla y que se caracterizan porque el electrón de más que va teniendo cada elemento respecto al anterior, no se añade en la última capa, si no (principalmente) en el nivel energético 5f, con lo que todos los actínidos tendrán, por un lado, 2 electrones en la Capa de Valencia, y por otro, un electrón extra por ahí (en el orbital f), que les dotará de unas características especiales. Aunque su característica principal quizá sea que son muy radiactivos, todos ellos, con lo que su uso va venir determinado por esta última propiedad, que no tiene tanto que ver con que sean actínidos si no con sus pesados núcleos. El actinio, por ejemplo, tiene 89 protones y 138 neutrones en su núcleo. Además, los núcleos de estos elementos, cuantos más protones y neutrones tengan, menor será su radio. Respecto a otras características de los actínidos: Casi todos forman óxidos, con lo que en la naturaleza se encuentran unidos a otros elementos (Al menos los 8 primeros, porque el resto son todos de laboratorio).
La cantidad de actinio en la naturaleza es muy pequeña (se encuentra en muy pequeñas cantidades allí donde hay uranio (como 1 parte entre 10 millones)) con lo que, como comprenderás, este elemento fue descubierto hace relativamente poco. Tocaba descubrirlo a principios del siglo pasado, pues fue descubierto dos veces, una en 1899 por André-Louis Debierne, de quien hablé en la entrada del radio y en 1902 por Friedrich Oscar Giesel, un alemán que le dio el nombre de emanium, sin saber que ya había sido descubierto y nombrado. De todas maneras, no puso pegas, pues era un gran admirador de los Curie y aceptó de buen grado que le pusieran nombre desde el laboratorio parisino. Su nombre, por cierto, viene de las palabras en griego “alfa” y “rayos”.
Ambos científicos descubrieron el actinio a partir de la plecblenda, el mineral del uranio que, siempre además de éste elemento, contiene, entre otros: Radio, radón, polonio, etc. El caso es que, de todos ellos, el primero en ser aislado fue el actinio.
El actinio es un metal blanco plateado, pero sobretodo, es un elemento muy radiactivo, 150 veces más que el radio (Incluso brilla en la oscuridad con un tono azulado). Emite partículas alfa (convirtiéndose en francio) o partículas beta (pasando a ser torio) y su vida media (el tiempo en el que se desintegran la mitad de los átomos de una determinada muestra) es de 21773 años.
 |
| Brillo del actinio. El aire se ioniza y brilla. |
El elemento natural (Ac227) es demasiado escaso y con demasiado tiempo de vida como para que sea útil para algo. Pero para eso tenemos laboratorios o reactores nucleares: Para poder obtener elementos sintéticos y poder utilizarlos en algo. Por ejemplo, con 2 neutrones menos que el Ac227, obtenemos Ac225, que tiene una vida media de 10 días, lo cual es algo más útil. (Si el uranio emite una alfa, pasa a ser torio, que emite una beta y pasa a ser protactinio que si emite una alfa pasará a ser actinio. Mira más abajo la imagen de la Serie del actinio). Una pequeña muestra de este isótopo (Ac225) emitirá una enorme cantidad de partículas alfa. Y si necesitas partículas alfa, puede ser una buena opción. ¿Y para qué querría nadie tantas alfas? Pues como viene siendo habitual en estos casos: científicos de laboratorio o médicos (oncólogos, como los de Actinium Pharmaceuticals, por ejemplo).
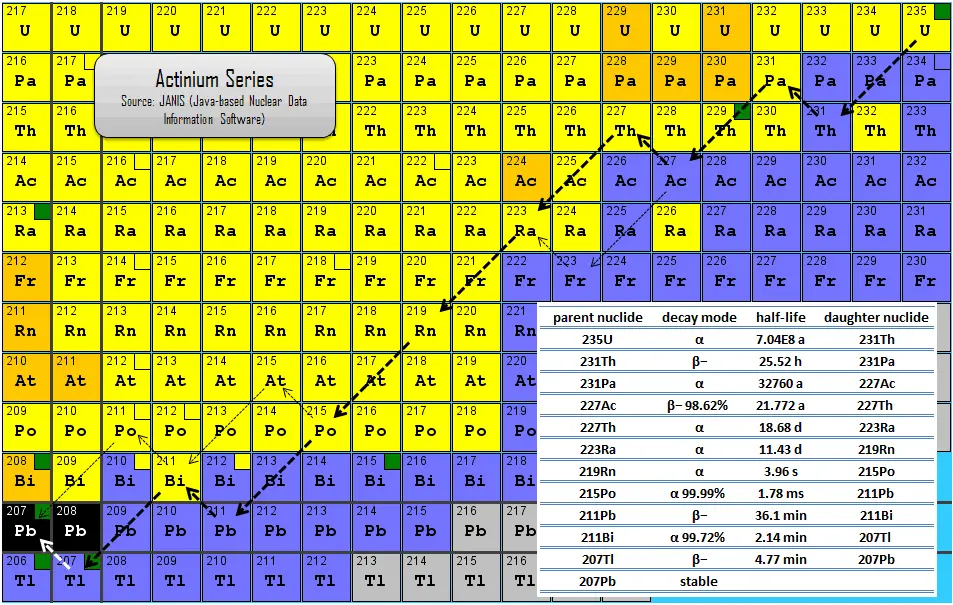
Por último, simplemente mostrarte la conocida como Serie del actinio, que comienza con el U235 (A su vez el U235 puede venir del plutonio 239, Pu239). El caso es que si un elemento emite una partícula alfa (dos protones, dos neutrones), como pierde 2 protones, se mueve dos elementos en la tabla. (El uranio tiene 92 protones y el torio 90). Si el torio emite una partícula beta negativa (un neutrón se convierte en un protón más un electrón), entonces gana un protón, con lo que pasa a ser protactinio (91 protones). El protactinio (Pa231) emite una partícula alfa pasando a ser actinio 227. Que sigue decayendo y transformándose en otros elementos según la cadena que se ve en la imagen inferior. Espectacular.
No hay comentarios:
Publicar un comentario